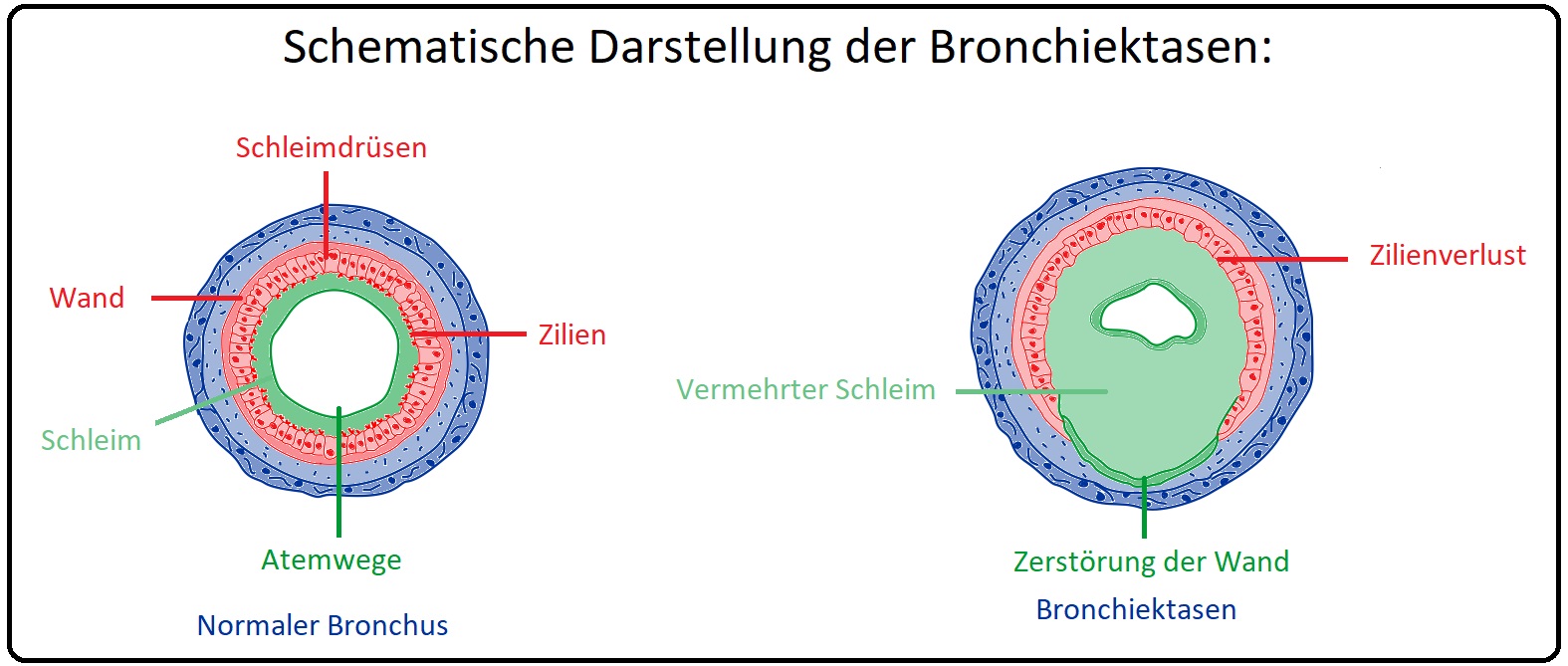
→ Definition: Bronchiektasen stellen irreversible zylindrische, sackförmige (= zystische) oder variköse Erweiterungen der mittleren bis distalen Bronchien dar, die angeboren oder häufiger erworben sein können. Während angeborene Bronchiektasen vor allem in den Lungenoberfeldern lokalisiert sind, findet man erworbene - in den -unterfeldern.
→ Epidemiologie:
→ I: Die Inzidenz der Entwicklung einer Bronchiektase liegt bei 60/100000 Einwohner.
→ II: Aufgrund der Impfungen und der gezielten Antibiotikatherapie ist diese chronische Atemwegserkrankung nur noch selten nachweisbar; es besteht eine deutlich rückläufige Tendenz.
→ Ätiologie: Nach ihrer Entstehung unterscheidet man zwischen:
→ I: Angeborenen Bronchiektasen: Sind mit 25% die seltener Form. Mögliche Ursachen:
→ 1) Anatomische Anomalien wie die Tracheobronchomalazie.
→ 2) Funktionell bei Mukoviszidose.
→ 3) Immunologisch beim IgA-Mangelsyndrom oder Alpha-Antitrypsin-Mangel.
→ 4) Bei der primär ciliären Dyskinesie.
→ II: Erworbene Bronchiektasen: Sie entstehen aufgrund einer entzündlichen Zerstörung der Wandstrukturen (elastisches Bindegewebe und Muskulatur) mit konsekutiver Narbenbildung bei:
→ 1) Rezidivierenden bronchopulmonalen bakteriellen oder viralen Infekten (z.B. Haemophilus influenzae, Adenoviren, Masernvirus, etc.) wie z.B. bei Bronchitis, Bronchiolitis, Pneumonie oder Lungentuberkulose,
→ 2) COPD,
→ 3) Bronchusstenose unterschiedlicher Genese (z.B. Bronchialkarzinom, Fremdkörperstenose, etc.) und
→ 4) Bronchopulmonale Aspergillose.
Pleuraschwarten, Hypogammaglobulinämie und andere Abwehrschwächen (z.B. "common-variable-immunodeficiency-syndrome", angeborenes Immunmangelsyndrom, etc.) begünstigen die Entstehung.
→ III: Sonderformen: Sind z.B:
→ 1) Das Kartagner-Syndrom: Wird autosomal-rezessiv vererbt und weist eine charakteristische Symptomtrias auf:
→ A) Situs inversus,
→ B) Fehlende Stirnhöhlen, Sinusitis, Nasenpolypen und
→ C) Bronchiektasen.
Pathophysiologisch fehlen bei den kontraktilen Fibrillen der Flimmerhaare, die für die Bewegung wichtigen Proteine, insbesondere die Dysneine. Betroffen hierbei sind die Flimmerhaare des Respirationstraktes sowie die Spermienschwänze
→ 2) Young-Syndrom: Autosomal-rezessiv vererbte Erkrankung mit sino-pulmonalen Infekten, Bronchiektasen und einer obstruktiven Azoospermie.
→ Pathogenese: Bei der Entstehung der Bronchiektasen steht die Störung der mukoziliären Clearance im Vordergrund. Folge ist eine gestörte Bronchialreinigung mit Sekretstau und konsekutiven pulmonalen Infekten aufgrund einer bakteriellen Besiedlung. Dies wiederum führt im Sinne einer chronischen Entzündung zur Destruktion der Schleimhaut mit anschließender Dilatation der Bronchialwände. Die erweiterten Bronchien erschweren zusätzlich das Ableiten des Bronchialsekretes, was wiederum die Ausbildung von Infekten begünstigt.
→ Pathologie: Nach morphologischen Aspekten unterscheidet man bei den Bronchiektasen zwischen:
→ I: Sackförmige Bronchiektasen: Sie bestehen aus unregelmäßige geweiteten, dicht nebeneinander liegende Bronchiallichtungen.
→ II: Zylindrische Bronchiektasen: Hierbei reicht die Bronchiallichtung ohne Verjüngung bis unter die Pleura. Durch narbige Einziehungen manifestiert sich ein variköses Aussehen.
→ Lokalisation: Die Bronchiektasen treten in 50% der Fälle beidseitig auf können aber auch einseitig oder diffus lokalisiert sein. Hauptlokalisation sind die Lungenunterlappen.
→ Klinik: Klassische Symptome sind insbesondere:
→ I: Chronisch produktiver Husten mit reichlich purulentem Sputum (= maulvolle Expektorationen), häufig morgens oder nach Lagewechsel.
→ II: Süßlich-übel-riechendes Sputum mit charakteristischer Dreischichtigkeit (Schaum-Schleim-Eiter).
→ III: Gerade im Erwachsenenalter zeigen sich Hämoptysen und Blutbeimengungen im Sputum.
→ IV: Endstadium: Hierbei entwickelt sich eine Symptomatik bestehend aus Zyanose, Einsatz der Hilfmuskulatur, Trommelschlegelfinger und Uhrglasnägel.
→ V: Bei akuter Exazerbation: Manifestieren sich Symptome wie Müdigkeit, Abgeschlagenheit, vermehrter Husten mit Auswurf, Fieber, Dyspnoe, verstärktes Giemen sowie mittel- bis grobblasige feuchte Rasselgeräusche.
→ Komplikationen: Wichtige und zum Teil schwerwiegende Komplikationen der Bronchiektasen sind u.a.:
→ I: Rezidivierende Infekte und Pneumonien, oftmals verursacht durch Pneumokokken-, Klebsiella-, Haemophilus influencae-, Pseudonomas-Infektionen (Staphylococcus aureus) sowie bronchopulmonaler Aspergillusbefall.
→ II: Atelektasen und Lungenabszess.
→ III: Weitere Ursachen: Sind:
→ 1) Septische Embolien mit der Gefahr des Hirnabszess oder der Sepsis.
→ 2) Lungenblutungen.
→ 3) Obstruktive Ventilationsstörungen mit konsekutiver respiratorischer Insuffizienz und das
→ 4) Cor pulmonale sind heutzutage nur noch selten anzutreffen.
→ Diagnose:
→ I: Anamnese/klinische Untersuchung: Abklärung rezidivierender Infekte in der Eigenanamnese, auskultatorisch zeigen sich feuchte Rasselgeräusche meist basal, inspektorisch evtl. Nachweis von Trommelschlegelfingern und Uhrglasnägeln oder einer zentralen Zyanose (sie zeichnet sich durch Blaufärbung der Körperperipherie und der zentralen Schleimhäute wie Zunge, Lippen, etc. aus).
→ II: Labor:
→ 1) Blutgasanalyse: Nachweis einer respiratorischen Partialinsuffizienz mit Hypoxämie mit pathologisch vermindertem pO2-Wert, bei normalem pCO2-Wert (Abb.: Normwerte der Blutgasanalyse).
→ 2) Bakteriologische Untersuchung des Sputums. Häufige Erreger sind u.a. Haemophilus influenza, Pseudonomas aeruginosa, Moxarella catarrhalis, Streptococcus pneumoniae und Staphylococcus aureus.
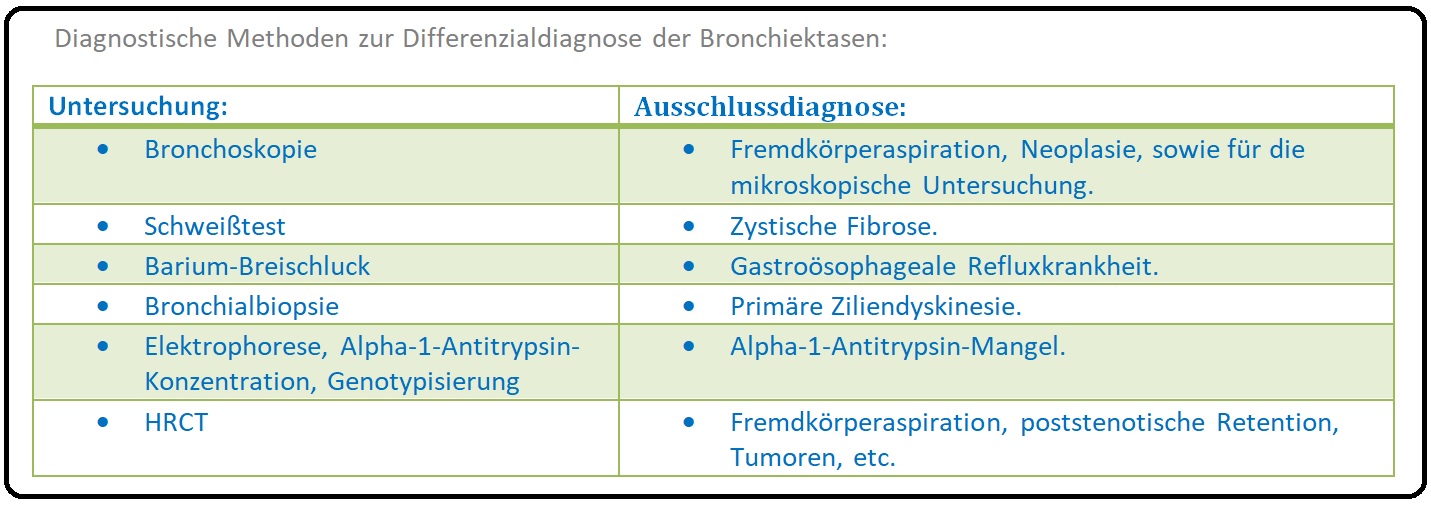
→ Klinisch-relevant: Zudem ist der Ausschluss einer:
→ A) Mukoviszidose,
→ B) Primären Ziliendyskinesie (mit Hilfe einer Nasenschleimhautprobe) und
→ C) Eines Immundefektes durch Bestimmung der Immunglobuline und Lymphozytenpopulation obligat.
→ III: Bildgebende Verfahren:
→ 1) Röntgen: Thorax in 2 Ebenen. Bei Sekretstau lokal betonte und vermehrte Lungenstrukturzeichnung, evtl. zystische Transparenzerhöhung mit evtl. Flüssigkeitsspiegeln. Des Weiteren möglicher Nachweis von Schienenzeichen (= Tramlines: Hierbei handelt es sich um parallel verlaufende, verdickte Bronchuswände). Im Spätstadium erfolgt die radiologische Darstellung einer Wabenlunge mit grob-retikulärer Netzzeichnung, infolge einer Verschmelzung der Azini und Alveolen zu Blasen und gleichzeitiger Fibrosierung des pulmonalen Interstitiums.
→ 2) HR-CT: Ist das Untersuchungsverfahren der 1. Wahl zur Diagnosebestätigung der Bronchiektasen. Hier besteht eine direkte Darstellung der betroffenen Bronchien mit:
→ A) Schienenphänomen: Im Längsschnitt Nachweis von parallel angeordnete Strukturen, die die verdickten Bonchialwände darstellen.
→ B) Siegelringphänomen: Charakteristische Ringstruktur mit kleineren direkt anliegenden Pulmonalarterien.
sowie des pulmonalen Parenchyms.
→ 3) Bronchoskopie: Zur Abklärung einer Bronchusstenose, evtl. kombiniert mit einer bronchopulmonalen Lavage zur Gewinnung von Material für die Erregerdiagnostik.
→ Differenzialdiagnose: Differenzialdiagnostisch müssen von den Bronchiektasen nachfolgende Erkrankungen abgegrenzt werden; hierzu zählen insbesondere:
→ I: Chronisch-obstruktive Bronchitis mit oder ohne Lungenemphysem (COPD).
→ II: Intrinsisches Asthma bronchiale.
→ Therapie: Im Vordergrund der Therapie steht die Sekretelimination sowie die Infektvorsorge bzw. -behandlung, um ein Fortschreiten der chronisch-pulmonalen Erkrankung zu verhindern:
→ I: Allgemeinmaßnahmen:
→ 1) Morgendliche Bronchialtoilette in Knie-Ellenbogenlagerung mit vollständigem Abhusten des Sputums.
→ 2) Externe Klopf- und Vibrationsmassage (mindestens 10min).
→ 3) Ausreichende Flüssigkeitszufuhr sowie
→ 4) Inhalation von Kochsalz.
→ II: Medikamentös:
→ 1) Applikation von Bronchospasmolytika und Mykolytika (z.B. Acetylcystein 3x 200mg).
→ 2) Eine aktive Immunisierung gegen Pneumokokken und Haemophilus influenza ist obligat.
→ 3) Gezielte antibiotische Therapie nach Antibiogramm. Als Initialtherapie empfiehlt sich eine Antibiotikatherapie mit Fluorchinolonen über einen Zeitraum von 3 Wochen. Bei bekanntem Pseudonomasbefall ist die Kombinationstherapie mit z.B. Piperacillin und Tobramycin oder Ceftazidim und Tobramycin indiziert. In schweren Fällen kann zur Reduktion der Exazerbation eine prophylaktische Antibiose-Behandlung (i.v.) erfolgen.
→ Klinisch-relevant: Bei initialem Fehlen des Antibiogramms erfolgt eine Breitbandantibiotikatherapie, die P. aeruginosa (gram-negatives Stäbchenbakterium) mit erfasst. Hierfür bieten sich Antibiotika wie Piperacillin/Tazobactam, Cefepim, Imipenem evtl. mit einem Makrolid kombiniert, aber auch Fluorchinolone wie Levofloxacin oder Ciprofloxacin an.
→ III: Chirurgisch: Eine operative Intervention ist indiziert z.B. bei Verschlechterung der Symptomatik trotz adäquater Therapie, schweren Lungenblutungen, Bestehen eines Aspergilloms oder lokal begrenzten Bronchiektasen. Es erfolgt eine Segmentresektion oder Lobektomie. Ultima ratio stellt die Lungentransplantation dar, die v.a. bei fortgeschrittener Erkrankung mit respiratorischer Insuffizienz, pulmonaler Hypertonie und Cor pulmonale indiziert ist.
→ Prognose:
→ I: Sie ist gerade von der Grunderkrankung und den adäquaten Therapieoptionen abhängig.
→ II: Insbesondere durch die gute Bronchialtoilette und die adäquate Antibiotikatherapie ist die Lebenserwartung zumeist nicht mehr eingeschränkt.